MIRAMA, Burkina Faso
Mortalité Infantile Reduite par l’Administration de Masse de l’Azithromycine

Contexte
La mortalité infantile demeure élevée au Burkina Faso malgré les progrès enregistrés au cours de ces dernières décennies, passant de 85‰ en 2006 à 49,41‰ en 2021 soit l’un des taux les plus élevés au monde.
Pour atteindre l’objectif de 25 décès d’enfants de moins de cinq ans pour 1 000 naissances vivantes, il s’est avéré urgent de mettre en place des interventions efficaces et d’améliorer les systèmes de santé.
Ce projet est mis en œuvre de juin 2021 à mars 2025 par le Ministère de la santé à travers la Direction de la santé de la famille en collaboration avec Helen Keller International et sur financement de la Fondation Bill et Melinda Gates.
Suite aux résultats de l’essai MORDOR, le Burkina Faso a adopté l’administration de masse de l’azithromycine aux enfants âgés de 1 à 11 mois couplée au journées vitamines A Plus (JVA+), avec un essai randomisé en double aveugle et contrôlé par placebo. Ce projet est mis en œuvre de juin 2021 à mars 2025 par le Ministère de la santé à travers la Direction de la santé de la famille en collaboration avec Helen Keller International et sur financement de la Fondation Bill et Melinda Gates.
Objectif global
L’objectif global de MIRAMA est d’évaluer l’impact de l’azithromycine biannuelle sur la mortalité infantile lorsqu’elle est intégrée de manière expérimentale dans la plateforme d’intervention JVA+ au Burkina Faso.
Objectif spécifique 1
Évaluer si l’azithromycine intégrée à la plateforme JVA+ réduit la mortalité chez les enfants âgés de 1 à 11 mois par rapport au placebo.
Objectif spécifique 2
- Comparer la prévalence au niveau des grappes de pneumocoques résistants aux macrolides dans les échantillons nasopharyngés prélevés sur des enfants âgés de 1 à 59 mois dans les grappes recevant de l’azithromycine par rapport aux grappes recevant un placebo.
- Comparer la charge des déterminants génétiques de la résistance aux macrolides dans les échantillons rectaux prélevés sur des enfants âgés de 1 à 59 mois dans les groupes recevant de l’azithromycine par rapport aux groupes recevant un placebo.
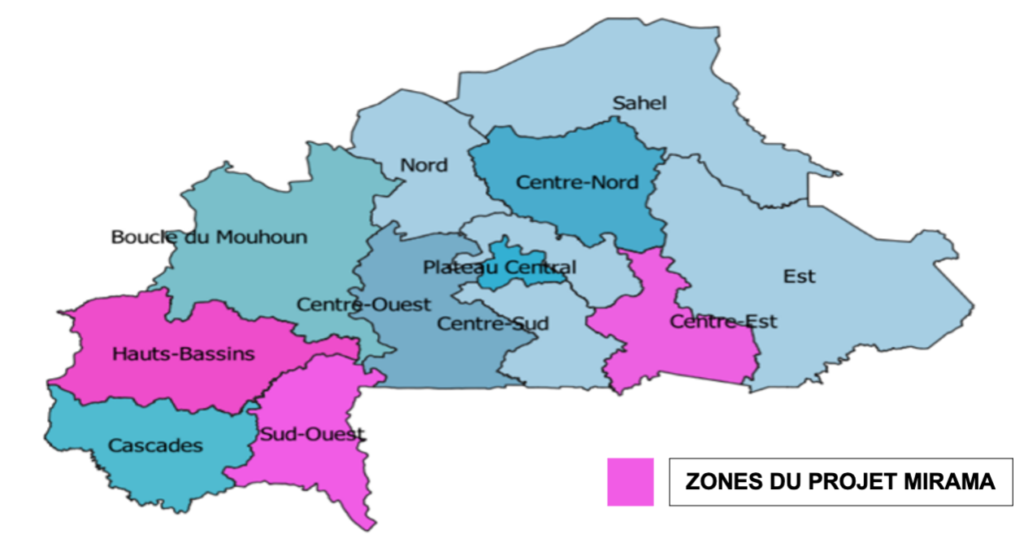
Méthodologie & Conception de l’étude
Zone d’étude
Les régions d’intervention sont les Hauts Bassins, Sud-Ouest et Centre-Est.
Mortalité
Il s’agit d’un essai randomisé en grappes, en double aveugle, contrôlé par placebo avec une répartition de 1 : 2 qui favorise le traitement actif. Toutes les communautés situées dans la zone ciblée sont sélectionnées pour participer à l’étude de mortalité.
Résistance
60 CSPS ont été sélectionnés au hasard de la zone d’étude pour recevoir un suivi de la résistance, en maintenant le ratio d’allocation 1 : 2. Dans chaque CSPS, une communauté a été sélectionnée au hasard pour la collecte d’échantillons. La surveillance de la résistance aux antimicrobiens a eu lieu avant la première distribution puis à la fin de la dernière distribution.
Taille de l’échantillon
20 districts, environ 2 595 villages avec près de 105 000 enfants âgés de 1 à 11 mois.
L’échantillon résistance
40 communautés azithromycine et 20 communautés placebo (répartition 2 : 1).
Autopsie verbale
À partir du 3ème recensement, une autopsie verbale est réalisée pour tous les enfants décédés identifiés lors des précédents recensements à l’aide du questionnaire VA 2016 de l’OMS. Les entretiens d’autopsie verbale ont été menés par du personnel formé par l’équipe du projet ainsi que du Centre de Recherche en Santé de Nouna.

Analyse statistique
Mortalité
L’analyse de la mortalité a été réalisée sous la forme d’une régression de Poisson ainsi que des méthodes standards pour les essais randomisés en grappes.
Résistance aux antimicrobiens
Les résultats mesurés sont :
- Prévalence des isolats pneumococciques résistants aux macrolides provenant d’échantillons nasopharyngés chez des enfants âgés de 1 à 59 mois, au départ et à 24 mois.
- Charge des déterminants génétiques de la résistance aux macrolides, y compris les déterminants connus pour être présents chez Campylobacter spp, Salmonella spp, Shigella spp et Escherichia coli, à partir d’échantillons rectaux d’enfants âgés de 1 à 59 mois, au départ et à la visite du 24ème mois.
Étude coût-efficacité
Une enquête a été réalisée pour déterminer le coût
du couplage de l’administration prophylactique de l’azithromycine aux JVA+. Le rapport de l’étude est en cours de finalisation.
Renforcement institutionnel
Un renforcement des capacités des différents participants/ acteurs a été effectué à tous les niveaux (central, intermédiaire, périphérique). L’équipe de coordination du projet a assuré la supervision des différentes formations et veillé à leur efficacité.
Des structures du ministère ont bénéficié d’infrastructures et d’équipement divers.
Comités de suivi et de surveillance
Deux comités ont été mis en place :
- Un comité technique de suivi qui s’est réuni une fois par trimestre pour assurer le suivi de la mise en œuvre du projet et une bonne coordination et collaboration avec les instituts et centres de recherche.
- Un comité de surveillance des données et de la sécurité (DSMB) qui s’est réuni une fois par an pour examiner les progrès de l’étude.
Principales réalisations
- 4 campagnes d’administration de masse de l’azithromycine intégrée à la plateforme JVA+
- 5 cycles de recensement et du suivi du statut vital dont le dernier est coupé avec l’historique des naissances
- 3 collectes de données de morbidité dans les centres de santé
- 3 enquêtes d’autopsie verbale
- • 2 enquêtes de collecte d’échantillons pour le suivi de l’antibio-résistance.
Calendrier de l’étude
L’ensemble des résultats de l’étude seront disponibles au premier trimestre de 2025.
Parties prenantes du projet MIRAMA
- Ministère de la santé
- Université de Californie, San Francisco (UCSF)
- Centre de Recherche en Santé de Nouna (CRSN)
Mise à l’échelle
La mise à l’échelle des activités de REACH a été validée par toutes les parties prenantes et les autorités compétentes.
Ce plan de passage à l’échelle de l’administration prophylactique de masse de l’azithromycine chez les enfants âgés de 1 à 11 mois au Burkina Faso, prévu pour la période 2024–2029, vise à couvrir progressivement les 70 districts des 13 régions du pays sur une période de six ans et sera entièrement intégré à la plateforme JVA+.

MIRAMA sur le terrain
Formation des Distributeurs communautaires sur les directives de mise en œuvre de l’administration d’Azithromycine en prélude à une Campagne JVA+ couplée à l’administration d’Azithromycine, Burkina Faso, Région du Sud-Ouest, juin 2022

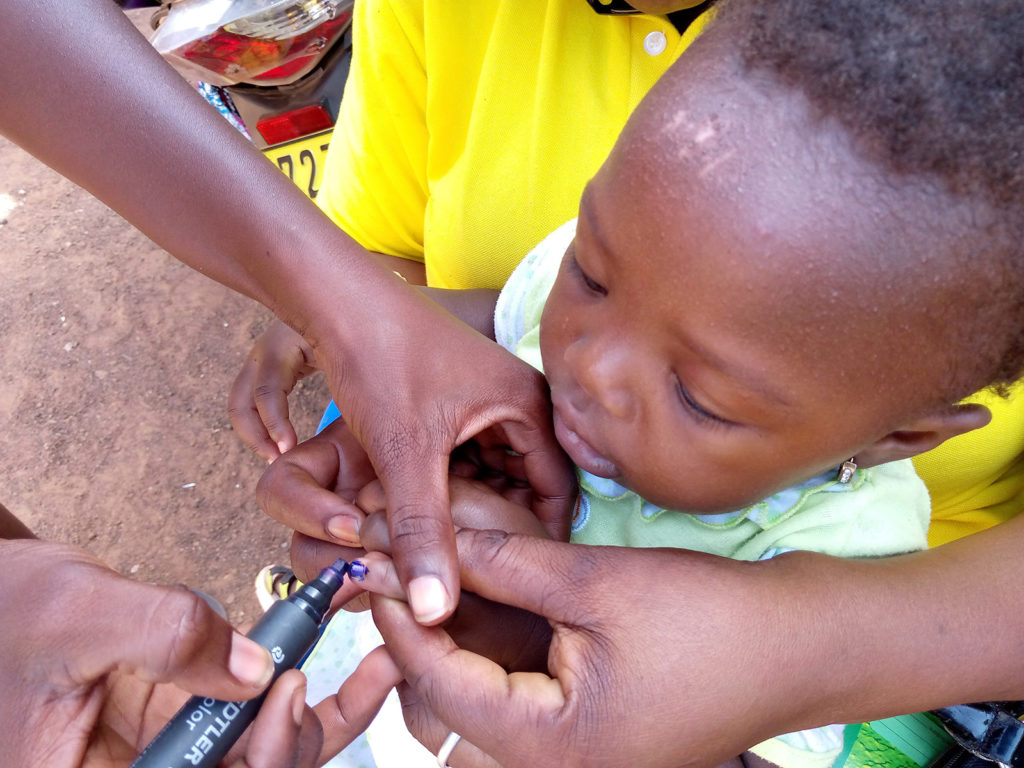
Marquage du doigt d’un enfant à l’encre indélébile après suivi son statut vital, Région du Sud-Ouest, Kampti, octobre 2022